¿Se puede fabricar diamantes artificiales ?
Nota: Este no es un experimento para realizar en casa o en el colegio, solo es para fines explicativos.
Este experimento no puede ser reproducido con facilidad debido a las extremas condiciones que requiere. Más que una idea para realizar un sábado por la tarde, este experimento está diseñado para explicar cómo es que un interesante fenómeno de la naturaleza puede ser reproducido en condiciones de laboratorio cuando se tiene el conocimiento y el equipo necesario. Para ello, necesitaremos explicar brevemente algunos conceptos que abordaremos a continuación:
¿Qué es el carbono?
El carbono es un elemento de la tabla periódica, muy común en el planeta Tierra pero relativamente poco común en el Universo. Es un elemento con propiedades muy interesantes debido a los electrones que posee y cómo se combina en complicadísimas formas para dar lugar incluso a seres vivos con otros elementos.
Características del carbono:
Normalmente existen 2 tipos de elementos: aquellos que ceden electrones y aquellos que reciben electrones. Muchos de los elementos buscan tener una configuración electrónica (cantidad de electrones totales) en la última capa de 8 electrones (o 2 para el caso del hidrógeno), lo que se conoce como la regla del octeto (que más que regla es una guía, ya que no todo se comporta de esta forma). Para ello, los átomos pueden captar o ceder electrones dependiendo de qué sea más sencillo energéticamente hablando.
Supóngase un elemento con 6 electrones, tendría dos caminos: podría o bien tomar 2 electrones de otro elemento o bien podría ceder sus 6 electrones. Dado que es más sencillo recibir 2 electrones que donar 6, entonces el elemento en cuestión seguramente arrancará 2 electrones en vez de cederlos. Por otro lado, supóngase un elemento con 2 electrones. Podría o bien ceder sus dos electrones o arrancar 6 a otro elemento. Dado que es más sencillo ceder dos electrones que arrancar 6, cederá sus electrones con mayor facilidad.
El carbono se encuentra en medio, tiene 4 electrones en la última capa o capa de valencia. Así, podría tanto arrancar como ceder 4 electrones, pero normalmente el carbono opta por “compartir” sus 4 electrones. Así, un oxígeno puede aportar 6 electrones y compartir 2 con el carbono, para que incluso otro oxígeno comparta los últimos dos electrones logrando que cada elemento tenga 8 electrones cada uno. También puede unirse a otros átomos de carbono así cada uno tendría 8, o bien con el hidrógeno, etc. Las posibilidades del carbono son muchísimas.
Particularidades del carbono
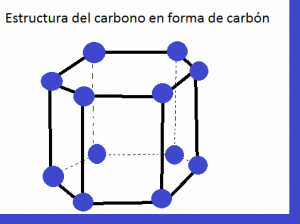
Cuando el carbono se encuentra en grandes cantidades con algunas impurezas, comenzará a “ordenarse” en forma de láminas hexagonales, que es uno de los sistemas cristalinos conocidos como redes de Bravais. Cuando esto sucede, el carbono es mucho muy frágil y puede fácilmente deslizarse una lámina sobre la otra. A condiciones normales de temperatura y presión como todas aquellas de la superficie terrestre el carbono adopta esta forma cuando se deposita como mineral (en los seres vivos hay enlaces complejos entre el carbono y otros elementos), a esta forma se le conoce como grafito. El hecho de que forme láminas que se deslicen con mucha facilidad es lo que nos permite escribir con la mina de los lápices.
A temperaturas extremadamente altas y presiones enormes el carbono comienza a expulsar de su red cristalina todas las impurezas y cambia de color gradualmente de negro a transparente. Ya sin las impurezas puede acomodarse en otro tipo de red muchísimo más resistente y entonces se forma lo que conocemos como diamantes. Dependiendo la pureza del mismo se determina la transparencia y así la dureza y calidad del diamante. Aunque los más puros se utilizan para joyería, los diamantes menos transparentes y sin valor para la joyería se utilizan para cortar, pulir, como agente abrasivo, para pulir y cortar otros diamantes, etc.
Diagramas de fase.
La pregunta natural siguiente sería: ¿Qué determina que el carbono se convierta en grafito o diamante? La respuesta es: las condiciones de temperatura y presión a las que se encuentra. Los diagramas de fase sirven para predecir precisamente qué fase tendrá un determinando elemento, compuesto, aleación o material a ciertas condiciones de temperatura y presión. A continuación se muestra un diagrama de fases, el del carbono y se explica brevemente cómo se interpretan estos diagramas:
Analizando el diagrama
Este es un diagrama muy sencillo. Muestra las regiones en las que se puede tener carbono en forma de diamante, en forma de grafito, vapor, líquido y otra forma conocida como carbono III. Cada región determina si a ciertas condiciones de temperatura se tendrá uno u otro. Incluso a ciertas condiciones se pueden tener tanto diamante como grafito mezclados, así como diamante y carbono III.
El diagrama anterior muestra que se pueden formar diamantes a temperaturas muy altas y presiones enormes, pero la presión requerida disminuye conforme se aumenta la temperatura (toda la línea que divide la región denotada como diamante + grafito de la región de grafito).
El diagrama anterior también muestra un hecho muy curioso, que aquello de que los diamantes son para siempre en realidad no es del todo cierto. Si se observa a condiciones normales (cercanas a 1 atm y 25 grados centígrados o 298 kelvin) no se debiese tener diamantes sino grafito. De hecho, todos los diamantes se están convirtiendo en grafito. Esta es una muy buena oportunidad para hablar de dos conceptos, el de velocidad o cinética y espontaneidad. En realidad el proceso por el cual el diamante vuelve a ser grafito es muy espontáneo, pero es extremadamente lento. Espontáneo significa que sucede por sí solo de forma natural y la cinética se refiere a qué tan rápido sucede. Mientras que el proceso se da de forma natural muy fácilmente, el tiempo que le toma a un diamante el convertirse nuevamente en grafito es de millones de años.
Ahora hagamos el experimento…
Materiales:
Para este experimento hipotético necesitaríamos:
- Bastante grafito (o carbón)
- Un contenedor muy resistente
- Mucha dinamita
- Un objeto muy pesado y resistente que comprima al grafito
Procedimiento:
Las condiciones de temperatura y presión tan grandes normalmente solamente se encuentran en dos escenarios de la naturaleza: cuando colisionan dos placas tectónicas exponiendo el magma del interior de la corteza terrestre y cuando se forma un volcán que penetra lo suficiente dentro de la corteza terrestre (entre 100 y 200 kilómetros de profundidad).
Sin embargo, gracias a los diagramas de fase podemos engañar a la madre naturaleza para producir diamantes artificiales. Con una gran explosión que empuje un material suficientemente pesado y resistente, comprimiendo así el carbón, se pueden alcanzar las temperaturas y presiones suficientes, así se puede (y de hecho se realiza en la industria) producir diamantes de forma artificial. Si bien nunca podrían llegar a ser diamantes de joyería, son más que suficiente para uso industrial.





gracias por la información es muy clara voy a comentar con mis alumnos de secundaria..y mi familia.
muy buenos los esperimentos para el cole!!!